ACIDO SOLFORICO (tecnica), 98%, L
5,00 €
Acido solforico, CAS 7664-93-9, solfato di idrogeno, INCI ACIDO SOLFURICO, Olio di vetriolo, Acidum sulphuricum, Acide sulphurique.
Parametro | Proprietà |
Acido solforico | Acido solforico, solforicodi idrogeno, Olio di vitriolo, Acidum sulphuricum, Acide sulphurique |
Formula | H2SO4 |
Struttura | 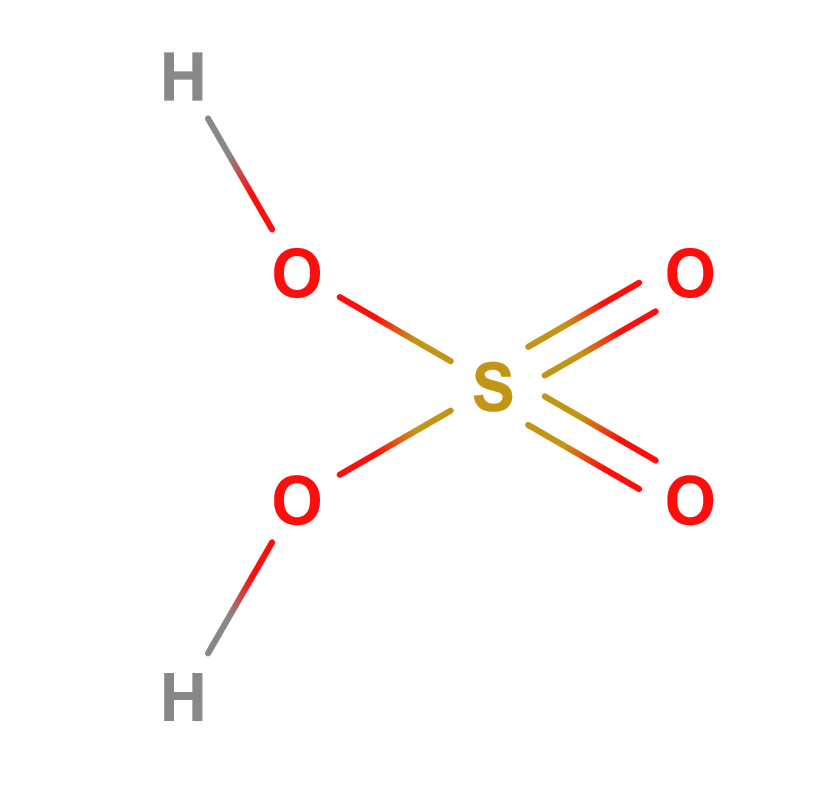 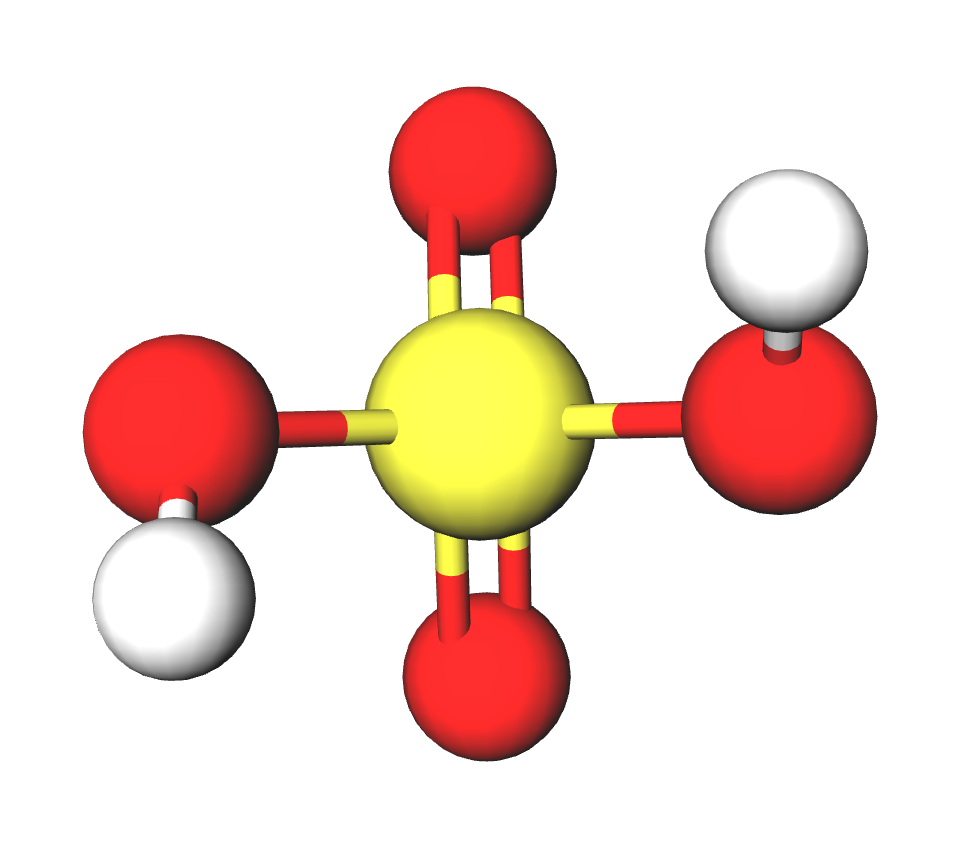 |
IUPAC | Acido solforico (acido solfato) – sulfuric acid (Tetraoxosulphate (VI) acid) |
INCI | SULFURIC ACID |
CAS | 7664-93-9 |
Massa molare | 98,079 g/mol |
Densità | 1.8302 g/cm3 (98%) |
Solubilità | Si mescola con acqua in qualsiasi proporzione, genera un calore elevato. |
L'acido solforico è un acido inorganico (minerale) forte con formula H2SO4. È un liquido viscoso incolore, a volte leggermente giallastro, che si mescola all'acqua in tutte le proporzioni. A volte il colore può essere più scuro a causa di impurità organiche o specificamente per avvertire le persone dei pericoli di questo liquido.
In agricoltura e orticoltura, l'acido solforico viene utilizzato per raccogliere le patate. Alcuni giorni prima del raccolto, i campi di patate vengono spruzzati con una soluzione di acido solforico per far diventare neri gli steli e le foglie delle patate. In questo modo si asciugano e non si impigliano negli attrezzi durante la raccolta. Per la raccolta delle colture alimentari si utilizza una soluzione acquosa contenente una combinazione di urea e acido solforico. Quest'ultimo ha un rapporto molare compreso tra 1:4 e 7:4. La composizione di questi elementi è ad azione rapida, non tossica e relativamente innocua per le attrezzature e l'ambiente. Questo metodo evita la penetrazione di sostanze tossiche nei prodotti alimentari, provoca danni significativamente minori alle colture ed è molto più rapido ed efficiente. Questa combinazione è particolarmente adatta per la raccolta precoce di patate e barbabietole. Concentrazioni molto basse di urea e acido solforico possono causare una significativa essiccazione delle foglie delle piante. Concentrazioni più elevate favoriscono un'essiccazione più rapida e riducono il rischio di perdita di sostanze attive dalle foglie. Le soluzioni con un contenuto di acido solforico pari a circa il 5% in peso sono le più adatte, mentre le soluzioni con una combinazione di urea e acido solforico pari al 10% in peso sono generalmente utilizzate a tassi di irrorazione inferiori. Le soluzioni vanno normalmente spruzzate sul fogliame a una dose minima di circa 22,5 kg/ha, tenendo conto del contenuto totale di urea e acido solforico. Un drenaggio più rapido si ottiene con una dose di circa 56 kg/ha, mentre con una dose di circa 336 kg/ha le foglie di tutte le specie di colture muoiono particolarmente rapidamente. In genere, l'irrorazione dopo 24 ore o prima, a dosi comprese tra 56 e circa 560 kg/ha, facilita notevolmente la raccolta. In agricoltura, l'acido solforico viene utilizzato per acidificare l'acqua utilizzata per l'irrigazione delle piante acidofile.
Acido | Concentrazione | g/m3 di acqua neutralizzata con 50 ppm di alcalinità | ml/m3 di acqua neutralizzata con 50 ppm di alcalinità | Elemento ricevuto |
Zolfo a. | 98 | 37.98 | 69.88 | 16.1 ppm S |
L'uso dell'acido solforico per abbassare il pH dell'acqua di irrigazione è molto vantaggioso al termine di un periodo di intensa crescita delle piante, quando è necessario un pH basso ma la crescita delle piante non deve più essere stimolata, e anche l'aspetto economico è rilevante. In orticoltura, l'acido solforico viene utilizzato per ridurre le malattie e i parassiti che attaccano le piantine abbassando il pH del terreno, riducendo così la crescita dei microrganismi nel suolo.
Nell'industria del legno, l'acido solforico viene utilizzato per annerire il legno di circa il 5-10%. Le bruciature chimiche che ne derivano hanno un aspetto simile a quello delle bruciature da fuoco, con la differenza che in questo caso è possibile ottenere l'oscurità desiderata, dal marrone chiaro al nero, e mettere in evidenza e mantenere le venature del legno. L'annerimento con acido solforico è molto meno dannoso per la superficie rispetto alla bruciatura a fuoco. Si consiglia di effettuare una prova in un'area a bassa visibilità prima di trattare il legno.
Nell'industria metallurgica, l'acido solforico è utilizzato come acido forte nell'industria dell'estrazione dei metalli preziosi per cambiare lo stato dei metalli preziosi da solido a ionico (liquido), sia per dissoluzione che come mezzo per una cella galvanica. Nelle arti metallurgiche, l'acido solforico viene utilizzato per annerire i metalli (con il ferro forma l'ossido di ferro II, che è passivo e di colore nero. Questo non solo produce un colore nero del metallo, ma fornisce anche un rivestimento protettivo del metallo. A volte l'acido solforico viene utilizzato per la finitura di prodotti di fabbro, come le spade, per far risaltare la struttura del metallo. Nella scultura dei metalli, l'acido solforico viene utilizzato per ossidare vari metalli per dare un effetto di metallo invecchiato. Le soluzioni di acido solforico sono utilizzate per passivare la superficie dell'alluminio, ad esempio nella produzione di alluminio anodizzato.
Nei laboratori, l'acido solforico viene utilizzato come catalizzatore in varie reazioni. Ad esempio, è un comune catalizzatore acido per la conversione del cicloesanone ossima in caprolattame, utilizzato nella produzione di nylon. Viene utilizzato per produrre acido cloridrico dal sale con il processo di Mannheim. Nella raffinazione del petrolio, ad esempio come catalizzatore nella reazione tra isobutano e isobutilene per produrre isoottano, un composto che aumenta il numero di ottani della benzina.
Nell'industria dei fertilizzanti, l'acido solforico è utilizzato nella produzione di acido fosforico, fosfati e fertilizzanti fosfatici. Le apatiti (minerali fosfatici) vengono trattate con acido solforico per produrre solfato di calcio e acido fosforico e, come intermedi, idrogenofosfato di calcio e/o diidrogenofosfato di calcio (altrimenti noto come superfosfato). In questo modo i minerali insolubili vengono trasformati in minerali solubili, che possono già essere assorbiti dalle piante.
Ca3(PO4)2(k) + 2H2SO4(aq) + 4H2O(s) → Ca(H2PO4)2(k) + 2CaSO4 ∙ 2H2O(k)
Il solfato di ammonio, ottenuto neutralizzando l'ammoniaca con l'acido solforico, può essere utilizzato come fertilizzante azotato. Questo processo viene solitamente effettuato nelle acciaierie, dove le alte temperature producono ammoniaca, che viene legata dall'acido solforico e può essere precipitata in polvere. I cristalli sono di colore marrone a causa delle impurità di ferro.
Nelle batterie, l'acido solforico viene utilizzato come elettrolita nelle batterie al piombo. Le soluzioni più comuni sono il 33,5% nelle batterie delle autovetture (1,25-1,28 g/ml) e/o il 37,52% nelle batterie dei macchinari industriali (1,285 g/ml).
Nel trattamento delle acque, l'acido solforico viene utilizzato per regolare il pH come strumento economico e molto efficace. Abbassando il pH del mezzo idrico a 7, è possibile eliminare il sapore sgradevole di sodio/soda e aumentare l'efficacia della disinfezione con l'uso di composti di cloro. Inoltre, riduce il rischio di corrosione dei sistemi, poiché a pH superiori a 9 rame, zinco, alluminio, ferro, ecc. possono iniziare a corrodersi. L'uso dell'acido solforico aiuta a separare le emulsioni nell'acqua (olio/acqua) in fasi distinte, aumentando così l'efficienza della pulizia. L'uso dell'acido solforico riduce la durezza dell'acqua (1 mole di acido solforico reagisce con 2 moli di calce). Questo acido può essere utilizzato anche nella rigenerazione dei filtri di addolcimento dell'acqua per rimuovere i depositi metallici sulla cartuccia del filtro.
Nell'industria alimentare, l'acido solforico viene utilizzato come ausiliario tecnico e come additivo nell'E513, nella produzione di formaggi, nonché negli zuccherifici e per la purificazione dell'acqua potabile, nella produzione di amido modificato e nella produzione di speciali proteine del siero di latte necessarie per i prodotti di sviluppo muscolare. L'acido solforico può essere utilizzato in due modi: come eccipiente tecnico o come additivo all'E513, che è innocuo per la salute. Nel primo caso, non è necessario specificare l'uso dell'acido solforico. Nel secondo caso, deve essere indicato nell'elenco degli additivi. L'acido solforico destinato all'industria alimentare deve essere conservato in contenitori speciali per evitare contaminazioni. L'acido solforico E513 è rigorosamente separato dall'acido utilizzato solo per scopi tecnici. L'acido solforico non viene aggiunto specificamente agli alimenti come conservante. Tuttavia, come agente regolatore del pH, è considerato un additivo alimentare di uso generale e viene utilizzato per controllare direttamente il pH durante la lavorazione degli alimenti, inibendo la crescita batterica e microbica. L'acido solforico è utilizzato nella produzione di acidi alimentari (ad esempio acido citrico e acido lattico) e nella regolazione del pH degli alimenti durante la lavorazione. L'acido solforico è consentito fino a un massimo dello 0,014% nelle bevande alcoliche e dello 0,0003% nei formaggi. Come additivo alimentare viene utilizzato nella produzione di estratto di luppolo modificato e come riduttore di pH per l'amido modificato. Utilizzato anche nel processo di estrazione, in particolare l'acido solforico, per regolare l'acqua utilizzata per estrarre i fucoidani dalle alghe brune. Il fucoidano è un polisaccaride solfatato utilizzato come ingrediente negli integratori alimentari.
Nell'industria della pulizia, l'acido solforico viene utilizzato in grandi quantità nell'industria siderurgica per rimuovere la ruggine e le incrostazioni dai prodotti in acciaio. L'aggiunta di perossido di idrogeno alla soluzione di acido solforico produce una “soluzione Piranha”, molto forte ma allo stesso tempo molto tossica. Questa miscela viene comunemente utilizzata per incidere i componenti elettronici o, nei laboratori, per pulire la vetreria. L'acido solforico si trova in alte concentrazioni negli scovolini acidi per sciogliere lo sporco, i capelli o disintegrare le salviette di carta.
Nelle scuole, l'acido solforico viene utilizzato come catalizzatore in molte reazioni in cui è necessario rimuovere l'acqua dalla reazione. Si tratta di nitrazione, esterificazione, scissione, essiccazione o altri tipi di reazioni. L'acido solforico viene utilizzato per rimuovere l'acqua dagli zuccheri e formare una struttura solida di carbonio. C11H22O11(k) → 12C(k) + 11H2O(d). Questo esperimento è noto anche come “Drago Nero”.
Importante: aggiungi il prodotto al carrello, compila i dati del modulo destinatario e conferma l'ordine. Grazie!
Per risparmiare il tuo prezioso tempo, consegneremo i prodotti ordinati all'indirizzo indicato e nell'orario a te più comodo!
*- Le immagini dei prodotti possono differire dall'aspetto reale del prodotto e della sua confezione, colore, completezza o forma. Le informazioni nella descrizione del prodotto sono di natura generale e potrebbero non corrispondere alle informazioni riportate sulla confezione, né rappresentano un metodo preciso di utilizzo del prodotto. I dati indicati relativi a prezzi e disponibilità dei prodotti possono in alcuni casi differire dai prezzi e dalle giacenze effettive.
**- Regolamento di esecuzione (UE) 2019/1148 del Parlamento europeo e del Consiglio, del 20 giugno 2019, relativo al commercio e all'uso di precursori di esplosivi, che modifica il regolamento (CE) n. 1907/2006 e abroga il regolamento (UE) n. 98/2013 (GU L 186 dell'11.7.2019, pag. 1). Il prodotto deve essere venduto solo a persone giuridiche, agricoltori o lavoratori autonomi con un'autorizzazione all'acquisto firmata e un uso legale.
Parola di avvertimento: Pericolo |
Pittogrammi di pericolo:
|
Frasi di pericolo (H-phrases): H314 Brucia gravemente la pelle e danneggia gli occhi. |
Frasi di prudenza (P-phrases): P102 Conservare fuori dalla portata dei bambini. P223 Tenere lontano da ogni possibile contatto con l'acqua, poiché il prodotto è altamente reattivo e può provocare un incendio. P260 Non inalare i vapori/aerosol. P280 Indossare guanti protettivi/indumenti protettivi/utilizzare protezioni per gli occhi/il viso. P301+P330+P331 IN CASO DI PERICOLO: Sciacquare la bocca. NON indurre il vomito. P303+P361+P353 IN CASO DI CONTATTO CON LA PELLE (o con i capelli): rimuovere immediatamente tutti gli indumenti contaminati. Lavare la pelle con acqua/urina. P305+P351+P338 IN CASO DI CONTATTO CON GLI OCCHI: lavare delicatamente con acqua per alcuni minuti. Rimuovere le lenti a contatto, se presenti e se è facile farlo. Continuare a lavare gli occhi. P405 Conservare sotto chiave. |
Prodotti correlati
(8 altri prodotti della stessa categoria)










